Les cathinones de synthèse: fiche drogue
Les cathinones de synthèse: fiche drogue
Les cathinones de synthèse sont apparentées à la molécule-mère cathinone (figure 1), l’un des principes psychoactifs du khat (Catha edulis Forsk). Les dérivés de la cathinone sont les β-céto (βc) analogues d’une phénéthylamine correspondante. Le groupe comprend plusieurs substances qui ont été utilisées en tant que principes pharmaceutiques actifs médicamenteux, par exemple, l’amfépramone (diéthylpropion; figure 2). Depuis le milieu des années 2000, des dérivés de la cathinone substitués sur le cycle, non réglementés, sont apparus sur le marché européen des drogues récréatives. Les cathinones les plus couramment disponibles sur ce marché jusqu’en 2010 semblaient être la méphédrone (figure 3) et la méthylone (figure 4). On trouve généralement ces produits sous forme de poudres blanches ou brunes avec un degré de pureté élevé. Les dérivés de la cathinone substitués sur le cycle auraient des effets similaires à ceux de la cocaïne, de l’amphétamine ou de la MDMA (ecstasy), mais leur pharmacologie détaillée est peu connue. En dehors de la cathinone (figure 1), de la méthcathinone (figure 5) ainsi que des deux composant pharmaceutique actifs l’amfépramone (figure 2) et la pyrovalérone, les dérivés de la cathinone ne font pas l’objet d’un contrôle international.
Chimie
Les figures 1 à 7 montrent la cathinone naturelle (figure 1) et six dérivés synthétiques (figures 2 à 7).
Figure 1: Cathinone
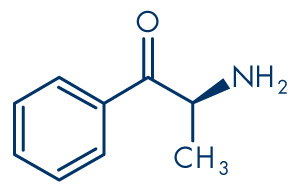
Formule moléculaire: C9H11NO
Poids moléculaire: 149.19 g/mol
Figure 2: Amfépramone (diéthylpropion)

Formule moléculaire: C13H19NO
Poids moléculaire: 205.30 g/mol
Figure 3: Méphédrone (4-méthylméthcathinone, 4-MMC)
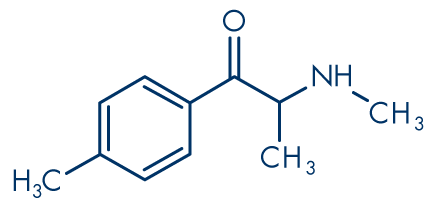
Formule moléculaire: C11H15NO
Poids moléculaire: 177.24 g/mol
Figure 4: Méthylone (β-céto-MDMA, 3,4-méthylènedioxy-N-méthylcathinone)

Formule moléculaire: C11H13NO3
Poids moléculaire: 207.22 g/mol
Figure 5: Méthcathinone (éphédrone)

Formule moléculaire: C10H13NO
Poids moléculaire: 163.22 g/mol
Figure 6: MDPV (3,4-méthylènedioxypyrovalérone)

Formule moléculaire: C16H21NO3
Poids moléculaire: 275.35 g/mol
Figure 7: Méthédrone (β-céto-PMMA, 4-méthoxyméthcathinone)

Formule moléculaire: C11H15NO2
Poids moléculaire: 193.24 g/mol
La cathinone (figure 1) et ses dérivés sont étroitement apparentés à la famille des phénéthylamines. Ainsi, la cathinone elle-même est la β-céto (βc) amphétamine, 2-aminopropiophénone ou, plus formellement, 2-amino-1-phényl-1-propanone (nom systématique UICPA). La première cathinone de synthèse apparue sur le marché des drogues récréatives, la méthcathinone (figure 5), est la β-céto-méthamphétamine, éphédrone ou N-méthylcathinone. La plupart des dérivés de la cathinone non réglementés qui ont été commercialisés ces dernières années sont substitués au niveau du cycle : le plus répandu étant probablement la méphédrone (4-méthylméthcathinone, 4-MMC, figure 3). Il est probable que certains produits vendus contiennent également un mélange de différents produits chimiques. Les autres cathinones signalées au système d’alerte précoce sur les nouvelles drogues comprennent la méthylone (β-céto -MDMA; 3,4-méthylènedioxy-N-méthylcathinone, figure 4), la MDPV (3,4-méthylènedioxypyrovalérone, figure 6), la méthédrone (β-céto -PMMA; la 4-méthoxyméthcathinone, figure 7) et la PPP (α-pyrrolidinopropiophénone).
Comme les phénéthylamines, les dérivés de la cathinone peuvent exister sous deux formes stéréoisomériques, qui peuvent avoir des puissances différentes. La cathinone présente à l’état naturel dans le khat est l’énantiomère S. Cependant, il est probable que la plupart des dérivés substitués au niveau du cycle soient des mélanges racémiques. On estime également que la racémisation de tous les dérivés de la cathinone peut se produire par tautomérie céto-énolique. La cathinone est labile et forme un dimère (la 3,6-diméthyl-2,5-diphénylpyrazine). Les dérivés de la cathinone peuvent également se réarranger via un dimère de dihydropyrazine pour former ce qu’on appelle des «isocathinones». Tous les dérivés connus de la cathinone sont soit N-alkylés ou ont l’atome d’azote qui fait partie d’un cycle pyrrolidine, et la plupart sont produits sous forme de sels de chlorhydrate. De nombreux produits illicites sont N-méthylés, c’est-à-dire des dérivés de l’éphédrone, et dès lors la méphédrone peut être décrite en tant que 4-méthyléphédrone. Les dérivés de la pyrrolidine (PPP, MDPV) peuvent être considérés comme un sous-ensemble de «designer drugs» partageant le même squelette que la pyrovalérone. Le tableau 1 dresse la liste des dérivés de la cathinone qui ont été utilisés comme composants pharmaceutiques actifs, trouvés dans des saisies de drogues, des échantillons collectés à des fins de contrôle ou mis en vente sur des sites internet (voir la figure 8). La naphyrone (1-naphthalèn-2-yl-2-pyrrolidin-1-ylpentan-1-one), un dérivé plus complexe de la cathinone, n’est pas incluse dans le tableau 1.
Figure 8: Structure générale d’un dérivé de la cathinone présentant des schémas de substitution

Tableau 1
Classification structurale des dérivés de la cathinone observés dans les saisies de drogues, les échantillons recueillis ou en vente sur des sites internet (voir la figure 8). Les composés qui sont ou ont été utilisés en tant que composants pharmaceutiques actifs (API) sont représentés en caractères gras.
| R1 | R2 | R3 | R4 | R5 | Nom |
| H | H | H | H | H | Cathinone |
| Méthyle | H | H | H | H | Méthcathinone (éphédrone) |
| Méthyle | Méthyle | H | H | H | N,N-Diméthylcathinone (métamfépramone) |
| Éthyle | H | H | H | H | N-Éthylcathinone (EC) |
| Méthyle | H | H | Méthyle | H | Buphédrone |
| Éthyle | H | 4-Méthyle | H | H | 4-Methyl-N-ethylcathinone |
| Méthyle | H | 4-Méthyle | H | H | Méphédrone (4-MMC; M-CAT) |
| Éthyle | Éthyle | H | H | H | Amfépramone |
| t-Butyle | H | 3-CI | H | H | Bupropion |
| Méthyle | H | 3,4-Méthylenedioxy | H | H | Méthylone (βk-MDMA) |
| Éthyle | H | 3,4-Méthylenedioxy | H | H | Éthylone (βk-MDEA) |
| Méthyle | H | 4-Méthyle | Methyle | H | Butylone (βk-MBDB) |
| Méthyle | H | 4-Méthoxy | H | H | Méthédrone (βk-PMMA) |
| Méthyle | H | 4-F | H | H | Fléphédrone (4-FMC) |
| Méthyle | H | 3-F | H | H | 3-Fluoromethcathinone (3-FMC) |
| {pyrrolidino} | H |
H |
H | α-Pyrrolidinopropiophénone (PPP) | |
| {pyrrolidino} | 4-Méthyle | H | H | 4-Méthyl-α-pyrrolidinopropiophénone (MPPP) | |
| {pyrrolidino} | 4-MeO | H | H | 4-méthoxy-α-pyrrolidinopropiophénone (MOPPP) | |
| {pyrrolidino} | 4-Méthyle | Propyle | H | 4-Méthyl-α-pyrrolidino-hexanophénone (MPHP) | |
| {pyrrolidino} | 4-Méthyle | Éthyle | H | Pyrovalerone | |
| {pyrrolidino} | 4-Méthyle | Methyle | H | 4-Méthyl-α-pyrrolidino-butyrophénone (MPBP) | |
| {pyrrolidino} | 4-Méthyle | H | Methyle | 4-Méthyl-α-pyrrolidino-α-méthylpropiophénone | |
| {pyrrolidino} | 3,4-Méthylenedioxy | H | H | 3,4-Méthylenedioxy-α-pyrrolidinopropiophénone (MDPPP) | |
| {pyrrolidino} | 3,4-Méthylenedioxy | Éthyle | H | 3,4-Méthylenedioxypyrovalérone (MDPV) | |
Forme physique
Les cathinones de synthèse se présentent le plus souvent sous forme de poudres amorphes ou cristallines blanches ou brunes, parfois en gélules. Contrairement à de nombreux dérivés de la phénéthylamine (MDMA, etc.), les comprimés sont moins courants, mais parfois disponibles sur le marché illicite, probablement en substitution à la MDMA.
Pharmacologie
Comme dans le cas des phénéthylamines, en l’absence de substitution sur le cycle, les cathinones se comportent comme des stimulants du système nerveux central (SNC), bien qu’invariablement avec une puissance inférieure à l’analogue correspondant de la phénéthylamine. Cette puissance plus faible provient du groupe β-céto qui crée une molécule plus polaire moins apte à passer la barrière hémato-encéphalique. Des études portant sur le métabolisme des dérivés de la méthcathinone chez les rats et les humains ont montré que ceux-ci sont N-déméthylés, le groupe céto est réduit en hydroxyle, et les groupes alkyles du cycle sont oxydés. Par ailleurs, peu d’études officielles ont été menées sur la pharmacocinétique ou la pharmacodynamique des cathinones substituées au niveau du cycle. D’après des observations de patients chez lesquels une intoxication à la méphédrone était suspectée, il apparaît que les dérivés de la cathinone présentent des effets sympathomimétiques similaires à ceux des dérivés d’amphétamine. Le premier cas mortel confirmé sur le plan toxicologique directement lié à la consommation de méphédrone a été enregistré en Suède en 2008.
Les rapports d’usagers sur les sites internet laissent entendre qu’une dose de méphédrone varie généralement entre 100 et 250 mg. En fonction de la substance particulière, les effets seraient similaires à ceux de la cocaïne, de l’amphétamine ou de la MDMA. Comme pour la cocaïne, l’euphorie très intense (état de «high») procurée par la méphédrone est de courte durée. Par conséquent, les usagers peuvent consommer plusieurs doses à la suite, jusqu’à 1 g en une session. Ceci a été confirmé lors de saisies de police au Royaume-Uni où le sachet de méphédrone le plus courant est proche de 750 mg.
Le cycle pyrrolidine et le groupe amine tertiaire tertiaire de la MDPV pourraient aboutir à une molécule plus lipophile, c’est-à-dire plus puissante; les forums d’usagers sur internet laissent à penser que la dose ne dépasse pas 5 à 10 mg. En outre, il est à noter que les p-méthoxyphénéthylamines (par exemple, PMA, PMMA) sont connues pour leur toxicité particulièrement élevée, et cette propriété pourrait se transmettre à leurs analogues β-céto. Par exemple, la méthédrone (p-méthoxyméthcathinone) a été détectée dans quelques cas de décès.
Synthèse et précurseurs
Les dérivés simples comme la méthcathinone et la N,N-diméthylcathinone peuvent être respectivement synthétisés par oxydation de l’éphédrine (ou pseudoéphédrine) et de la N-méthyléphédrine (ou N-méthylpseudoéphédrine). Il faut pour cela faire réagir le précurseur avec une solution de permanganate de potassium dans de l’acide sulfurique dilué. Les précurseurs peuvent être obtenus sous forme d’énantiomères spécifiques, permettant ainsi une synthèse stéréosélective. La cathinone elle-même peut être obtenue d’une manière similaire, à partir de la phénylpropanolamine (noréphédrine). L’un des risques du procédé au permanganate pour les usagers est une intoxication au manganèse si le produit n’est pas purifié.
Les dérivés de la N-méthylcathinone substitués au niveau du cycle sont synthétisés au mieux en faisant réagir la bromopropiophénone substituée de façon appropriée avec de la méthylamine; le résultat est toujours racémique. Dans le cas de la méthylone, par exemple, on peut préparer la 2-bromo-3,4-methylènedioxy-propiophénone en faisant réagir la 3,4-méthylènedioxypropiophénone avec du brome. Ces précurseurs sont facilement disponibles et aucun d’entre eux n’est sous contrôle international. D’autres méthodes sont nécessaires pour produire les dérivés de la pyrrolidine, mais à part la MDPV, des substances comme la PPP, la MPHP, la MOPPP et la MDPPP, qui ont fait une brève apparition en Allemagne en 2004 (voir le tableau 1), n’ont depuis été que rarement observées.
Mode de consommation
Certains usagers sniffent la méphédrone, mais la plupart des cathinones sont ingérées. Comme elles sont solubles dans l’eau, ces substances peuvent également être injectées. Du fait de leur labilité, les bases libres ne sont probablement pas fumables.
Autres dénominations
Afin de contourner d’éventuels contrôles, les fournisseurs de dérivés de cathinone les commercialisent souvent sous diverses appellations (par exemple Explosion, Blow, Recharge, etc.), en tant que «substances fertilisantes», «sels de bain», ou «produits chimiques destinés à la recherche», souvent accompagnés d’une mise en garde imprimée «non destiné à la consommation humaine». Comme dans le cas des phénéthylamines, les acronymes sont courants. Ainsi, MDPV correspond à 3,4-méthylènedioxypyrovalérone, 4-FMC à la 4-fluorométhcathinone (fléphédrone), et 4-MMC à la 4-méthylméthcathinone (méphédrone). Les noms d’usagers pour la méphédrone comprennent M-Cat, meph, drone, miaow, meow meow, subcoca-1 et bubbles; alors que la méthylone est parfois appelée Top Cat. Ces substances sont cependant fréquemment vendues dans des produits portant un grand nombre de noms qui changent rapidement avec le temps et dont le contenu spécifique n’est souvent pas indiqué. Les noms chimiques ordinaires peuvent prêter à confusion; ainsi, la méthylone, la méphédrone et la méthédrone doivent être distinguées les unes des autres et de la méthadone, analgésique narcotique non apparenté. Bien que la β-céto-MBDB soit souvent appelée «butylone», le terme butylone a également été utilisée comme marque commerciale pour le pentobarbital, un barbiturique non apparenté.
Analyse
Les dérivés de la cathinone ne produisent pas de réaction colorée avec le test de Marquis. Une analyse par chromatographie en phase gazeuse couplée à la spectromètrie de masse (GCMS) et par spectroscopie infrarouge (IR) n’est pas compliquée. Bien qu’il soit difficile de trouver dans le commerce des échantillons de référence purs de certains dérivés, des profils analytiques ont été publiés pour la plupart d’entre eux. Les tests portables immunosérologiques de la méthamphétamine donnent des réactions faussement positives avec certains dérivés de la cathinone.
Contrôle
Ces informations reflètent la situation au 19 juillet 2010.
La cathinone et la méthcathinone sont inscrites au tableau I de la Convention des Nations Unies de 1971 sur les substances psychotropes. L’amfépramone et la pyrovalérone sont inscrites au tableau IV de cette Convention, mais d’autres dérivés ne sont pas sous contrôle international. Quelques dérivés de la cathinone sont contrôlés dans certains États membres dans le cadre d’une réglementation sur les drogues ou d’une législation équivalente, par exemple: la méphédrone (Belgique, Danemark, Allemagne, Estonie, Irlande, France, Italie, Lituanie, Roumanie, Suède, Croatie et Norvège); la méthylone (Danemark, Irlande, Roumanie et Suède); la butylone (Danemark, Irlande, Roumanie, Suède et Norvège); la MDPV (Danemark, Irlande, Finlande et Suède); et la fléphédrone (Danemark, Irlande et Roumanie). Au Royaume-Uni, le contrôle générique couvre un large groupe de dérivés de la cathinone. La méphédrone est réglementée dans le cadre de la législation sur les médicaments aux Pays-Bas et en Finlande.
Usage médical
L’amfépramone et la pyrovalérone ont été utilisées comme anorexigènes, mais leur utilisation dans ce cadre est dorénavant obsolète. Le bupropion possède des propriétés antidépressives et est utilisé comme aide au sevrage tabagique.
Publications
Bibliographie
Archer, R. (2009) ‘Fluoromethcathinone: A new substance of abuse’, Forensic Science International 185 (1), p. 10–20.
Belal, T., Awad, T., De Ruiter, J. et Clark, C. R. (2009) ‘GC–IRD methods for the identification of isomeric ethoxyphenethylamines and methoxymethcathinones’, Forensic Science International 184, p. 54–63.
Bossong, M. G., Van Dijk, J. P. et Niesink ,R. J. (2005) ‘Methylone and mCPP: Two new drugs of abuse?’ Addiction Biology 10 (4), p. 321–323.
Camilleri, A., Johnston, M. R., Brennan, M., Davis, S. et Caldicott, D. G. E. (2010) ‘Chemical analysis of four capsules containing the controlled substance analogues 4-methylmethcathinone, 2-fluoromethamphetamine, alpha-phthalimidopropiophenone and N-ethylcathinone’, Forensic Science International 197 (1–3), p. 59–66.
Carroll, F. Y., Blough, B. E., Mascarella, S. W., et al. (2010) ‘Synthesis and biological evaluation of bupropion analogues as potential pharmacotherapies for smoking cessation’, Journal of Medicinal Chemistry 53 (5), p. 2204–2214.
Chintalova-Dallas, R., Case, P., Kitsenko, N. et Lazzarini, Z. (2009) ‘Boltushka: A homemade amphetamine-type stimulant and HIV risk in Odessa, Ukraine,’ International Journal of Drug Policy 20, p. 347–351.
Cozzi, N. V., Shulgin, A. T. et Ruoho, A. E. (1998) ‘Methcathinone (MCAT) and 2-methylamino-1-(3,4-methylenedioxyphenyl)propan-1-one (MDMCAT) inhibit [3H]serotonin uptake into human platelets’, American Chemical Society Division of Medicine Abstracts 215, p. 152.
Cozzi, N. V., Sievert, M. K., Shulgin, A. T., Jacob III, P. et Ruoho, A. E. (1998) ‘Methcathinone and 2-methylamino-1-(3,4-methylenedioxyphenyl)propan-1-one (methylone) selectively inhibit plasma membrane catecholamine reuptake transporters’, Society for Neuroscience Abstracts 24, p. 381–388.
Cozzi, N. V. Sievert, M. K., Shulgin, A.T., Jacob III, P. et Ruoho, A. E. (1999) ‘Inhibition of plasma membrane monoamine transporters by β-ketoamphetamines’, European Journal of Pharmacology 381, p. 63–69.
Dal Cason, T. A. (1997) ‘The characterization of some 3,4-methylenedioxycathinone (MDCATH) homologs’, Forensic Science International 87, p. 9–53.
Daly, M. (2010) ‘Teenage kicks’, Druglink 25 (1), p. 8–10.
Dickson, A. J., Vorce, S. P., Levine, B. et Past, M. R. (2010) ‘Multiple-drug toxicity caused by the coadministration of 4-methylmethcathinone (mephedrone) and heroin’, Journal of Analytical Toxicology 34 (3), p. 162–168.
Gibbons, S. et Zloh, M. (2010) ‘An analysis of the “legal high” mephedrone’, Bioorganic & Medicinal Chemistry Letters 20 (14), p. 4135–4139.
Gustavsson, D. et Escher, C. (2009) ‘Mefedron: Internetdrog som tycks ha kommit för att stanna’, Läkartidningen 106 (43), p. 2769–2771. English summary available at: http://www.lakartidningen.se/07engine.php?articleId=12986.
Kamata, H. T., Shima, N., Zaitsu, K. et al. (2006) ‘Metabolism of the recently encountered designer drug, methylone, in humans and rats’, Xenobiotica 36 (8), pp. 709–723.
Measham, F., Moore, K., Newcombe, R. et Welch, Z. (2010) ‘Tweaking, bombing, dabbing and stockpiling: The emergence of mephedrone and the perversity of prohibition’, Drugs and Alcohol Today, 2010, 10 (p. 14-21).
Meltzer, P. C., Butler, D., Deschamps, J. R. et Madras, B. K. (2006) ‘1-(4-Methylphenyl)-2-pyrrolidin-1-yl-pentan-1-one (pyrovalerone) analogues: A promising class of monoamine uptake inhibitors’, Journal of Medicinal Chemistry 49, p. 1420–1432.
Meyer, M. R., Peters, F. T. et Maurer, H. H. (2009) ‘Metabolism of the new designer drug mephedrone and toxicological detection of the beta keto designer drugs mephedrone, butylone and methylone in urine’, Annales de Toxicologie Analytique 21.
Meyer, M. R., Wilhelm, J., Peters, F. T. et Maurer, H. H. (2010) ‘Beta-keto amphetamines: Studies on the metabolism of the designer drug mephedrone and toxicological detection of mephedrone, butylone, and methylone in urine using gas chromatography–mass spectrometry’, Analytical and Bioanalytical Chemistry 397 (3), p. 1225–1233.
Nagai, F., Nonaka, R. et Kamimura, K. S. H. (2007) ‘The effects of non-medically used psychoactive drugs on monoamine neurotransmission in rat brain’, European Journal of Pharmacology 559 (2–3), p. 132–137.
Naoya, A., Kiyoshi, W. et Masahiko, F. (2006) ‘Role of dopaminergic system in the expression of methylone-induced behavioral effect in mice’. Bulletin of the Japanese Society for Neurochemistry 45(2–3), p. 301.
Power, M. (2010) ‘Mephedrone: The future of drug dealing?’, Druglink March/April 2010, Volume 25(1), p. 7–13.
Power, M. (2010) ‘World wired web’, Druglink 25 (1), p. 11–13.
Roussel, O., Perrin, M., Herard, P., Chevance, M. et Arpino, P. (2009) ‘La 4-méthyléphédrone sera-t-elle une “Ecstasy” du XXIème siècle?’, Annales de Toxicologie Analytique 21 (4), p. 169–177.
Shima, N., Katagi, M. et Tsuchihashi, H. (2009) ‘Direct analysis of conjugate metabolites of methamphetamine, 3,4-methylenedioxymethamphetamine, and their designer drugs in biological fluids’, Journal of Health Science 55 (4), p. 495–502.
Shimizu, E., Watanabe, H., Kojima, T. et al. (2007) ‘Combined intoxication with methylone and 5-MeO-MIPT’, Progress in Neuro-Psychopharmacology and Biological Psychiatry 31 (1), p. 288–291.
Springer, D., Fritschi, G. et Maurer, H. H. (2003) ‘Metabolism of the new designer drug α-pyrrolidinopropiophenone (PPP) and the toxicological detection of PPP and 4'-methyl-α-pyrrolidinopropiophenone (MPPP) studied in rat urine using gas chromatography-mass spectrometry’, Journal of chromatography. Analytical technologies in the biomedical and life sciences 796 (2), p. 53–66.
Springer, D., Fritschi, G. et Maurer, H. H. (2003) ‘Metabolism and toxicological detection of the new designer drug 3',4'-methylenedioxy-α-pyrrolidinopropiophenone studied in urine using gas chromatography-mass spectrometry’, Journal of chromatography. Analytical technologies in the biomedical and life sciences 793 (2), p. 377–388.
Springer, D., Fritschi, G. et Maurer, H. H. (2003) ‘Metabolism and toxicological detection of the new designer drug 4'-methoxy-α-pyrrolidinopropiophenone studied in rat urine using gas chromatography-mass spectrometry’, Journal of chromatography. Analytical technologies in the biomedical and life sciences 793 (2), p. 331–342.
Springer, D., Peters, F.T., Fritschi, G. et Maurer, H. H. (2003) ‘New designer drug 4′-methyl-α-pyrrolidinohexanophenone: Studies on its metabolism and toxicological detection in urine using gas chromatography–mass spectrometry’, Journal of chromatography. Analytical technologies in the biomedical and life sciences 789 (1), p. 79–91.
Springer, D., Staack, R. F., Paul, L. D., Kraemer, T. et Maurer, H. H. (2003) ‘Identification of cytochrome P450 enzymes involved in the metabolism of 4-methoxy-a-pyrrolidinopropiophenone (MOPPP), a designer drug, in human liver microsomes’, Xenobiotica 33 (10), p. 989–998.
Staack, R.F, .Fritschi, G. et Maurer, H. H. (2002) ‘Studies on the metabolism and toxicological detection of the new designer drug 4'-methyl-a-pyrrolidinopropiophenone in urine using gas chromatography-mass spectrometry’, Journal of chromatography. Analytical technologies in the biomedical and life sciences773 (1), p. 25–33.
Szendrei, K. (1980) ‘The chemistry of khat’, Bulletin on Narcotics 32 (3), pp. 5–35.
Uchiyama, N., Kikura-Hanajiri, R., Kawahara, N., et Goda, Y. (2008) ‘Analysis of designer drugs detected in the products purchased in fiscal year 2006’, Journal of the Pharmaceutical Society of Japan 128 (10), p. 1499–1506.
Westphal, F., Junge, T., Rösner, P., et al. (2006) ‘Mass spectral and NMR spectral data of two new designer drugs with an α-aminophenone structure: 4′-methyl-α-pyrrolidinohexanophenone and 4′-methyl-α-pyrrolidinobutyrophenone’, Forensic Science International 169 (1), p. 32–42.
Westphal, F., Junge, T., Rösner, P., Sönnichsen, F. et Schuster, F. (2009) ‘Mass and NMR spectroscopic characterization of 3,4-methylenedioxypyrovalerone: A designer drug with α-pyrrolidinophenone structure’, Forensic Science International 190 (1), p. 1–3.
Winstock, A. (2010) ‘Drugs survey’, Mixmag 14 January.
Winstock, A. R., Marsden, J. et Mitcheson, L. (2010) ‘What should be done about mephedrone?’, BMJ 340, p. c1605.
Wood, D., Davies, S., Puchnarewicz, M., et al. (2010) ‘Recreational use of mephedrone (4-methylmethcathinone, 4-MMC) with associated sympathomimetic toxicity’, Journal of Medical Toxicology, 1 April.
Wood, D. M., Davies, S., Puchnarewicz, M., et al. (2009) ‘Recreational use of 4-methylmethcathinone (4-MMC) presenting with sympathomimetic toxicity and confirmed by toxicological screening. Abstracts of the 2009 North American Congress of Clinical Toxicology Annual Meeting, September 21–26, 2009, San Antonio, Texas, USA’, Clinical Toxicology 47 (7), p. 733.
Zaitsu, K., Katagi, M., Kamata, H., et al. (2009) ‘Determination of the metabolites of the new designer drugs bk-MBDB and bk-MDEA in human urine’, Forensic Science International 188 (1–3), p. 131–139.
Zaitsu, K., Katagi, M., Kamata, H. T., Miki, A. et Tsuchihashi, H. (2008) ‘Discrimination and identification of regioisomeric β-keto analogues of 3,4-methylenedioxy-amphetamines by gas chromatography-mass spectrometry’, Forensic Toxicology 26 (2), p. 45–51.











